
اعتبار: © andriano_cz / Adobe Stock
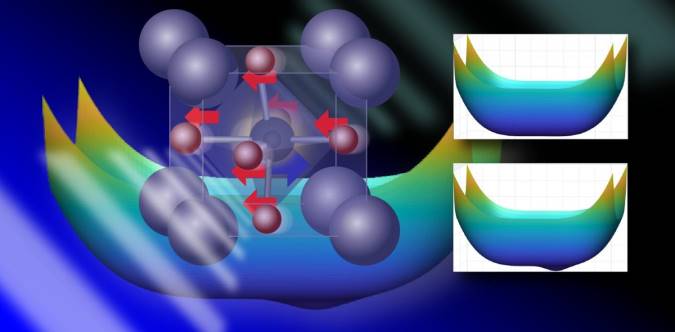
دانشمندان دانشگاه لیدز شکل جدیدی از طلا را ایجاد کرده اند که فقط دو اتم ضخامت دارد - نازکترین طلای بدون تکیه گاه که تاکنون ایجاد شده است.
محققان ضخامت این طلا را 47/0 نانومتر اندازه گیری کردند - این یک میلیون برابر نازک تر از ناخن انگشت انسان است. این ماده به عنوان ماده ای دو بعدی در نظر گرفته می شود زیرا فقط شامل دو لایه اتمی است که بر روی یکدیگر قرار گرفته اند. تمام اتمها اتمهای سطحی هستند - هیچ اتمی تنه ای پنهان در بین دو سطح وجود ندارد.
این ماده می تواند کاربردهای گسترده ای در تجهیزات پزشکی و صنایع الکترونیکی داشته باشد - و همچنین می تواند به عنوان یک کاتالیزور برای سرعت بخشیدن به واکنش های شیمیایی در طیف وسیعی از فرآیندهای صنعتی استفاده شود.
تست های آزمایشگاهی نشان می دهد که طلای فوق العاده نازک 10 برابر به عنوان یک بستر کاتالیزوری نسبت به نانوذرات طلای مورد استفاده در حال حاضر ، که موادی سه بعدی با اکثریت اتم های موجود در تنه و نه در سطح هستند ، کارآمدتر است.
دانشمندان معتقدند که این ماده جدید همچنین می تواند اساس آنزیم های مصنوعی را تشکیل دهد که می توانند در تست های تشخیصی پزشکی سریع و محتاطانه و در سیستم های تصفیه آب مورد استفاده قرار گیرند.
اعلامیه ای مبنی بر این که این فلز فوق العاده نازک با موفقیت تولید شده است در ژورنال علوم پیشرفته منتشر شده است.
نویسنده راهبر مقاله ، دکتر سونجی یِ ، از گروه فیزیک مولکولی و نانو مقیاس لیدز و موسسه تحقیقات پزشکی لیدز ، گفت: "این کار تا حد یک دستاورد برجسته می رسد."
"نه تنها این امکان را فراهم می کند که بتوان از طلا در فن آوری های موجود به طور مؤثر استفاده کرد ، بلکه مسیری را فراهم می کند که به دانشمندان علوم مواد امکان می دهد فلزات دو بعدی دیگر را توسعه دهند."
"این روش می تواند تولید نانومواد را نوآوری کند."
تیم تحقیق به دنبال همکاری با صنعت در مورد روش های مقیاس گذاری روند هستند.
سنتز نانو ورقه طلا در محلول آبکی صورت می گیرد و با اسید کلروآوریک ، ماده معدنی حاوی طلا شروع می شود. این ماده در حضور یک "عامل محدود کننده" به فرم فلزی آن کاهش می یابد – مادهای شیمیایی که طلا را تشویق می کند تا به صورت یک ورق به ضخامت تنها دو اتم شکل بگیرد.
به دلیل ابعاد نانو مقیاسی طلا ، در آب سبز به نظر می رسد - و با توجه به شکل آن ، محققان آن را نانو جلبک دریایی توصیف می کنند.
تصاویر گرفته شده از یک میکروسکوپ الکترونی نحوه تشکیل اتم های طلا را به یک شبکه بسیار سازمان یافته آشکار می کند. تصاویر دیگر، نانو جلبک دریایی را نشان می دهد که به طور مصنوعی رنگ شده است.
پروفسور استفان ایوانز ، رئیس گروه تحقیقاتی مولکولی و نانو مقیاس که سرپرستی این تحقیق را بر عهده داشت ، گفت: بهره های قابل توجهی که می توان از استفاده از این ورق های طلای فوق العاده نازک حاصل کرد ، نتیجه مهم نسبت سطح زیاد به حجم است.
وی گفت: "طلا یک کاتالیزور بسیار مؤثر است. از آنجا که نانو ورقه ها بسیار نازک هستند ، درست تقریباً هر اتم طلا نقشی در کاتالیزوری بازی می کند. این بدان معنی است که این فرایند بسیار کارآمد است."
تست های محک استاندارد آشکار کرد که ورقه های نانو مقیاس طلا ده برابر بیشتر از نانوذرات طلا که معمولاً در صنعت استفاده می شوند ، کارآمد هستند.
پروفسور ایوانز اظهار داشت: "داده های ما نشان می دهد که صنعت می تواند همان تأثیر را از استفاده از مقدار کمتری طلا به دست آورد ، و این هنگامی که در باره یک فلز گرانبها صحبت می کنید دارای مزایای اقتصادی است."
تست های محک مشابه نشان داد که ورق های طلا می توانند به عنوان آنزیم های مصنوعی بسیار مؤثر عمل کنند.
پوسته ها همچنین انعطاف پذیر هستند ، به این معنی که می توانند اساس اجزای الکترونیکی برای صفحه های قابل خمش ، جوهرهای الکترونیکی و نمایشگرهای رسانای شفاف را تشکیل دهند.
پروفسور اوانز فکر می کند که به ناچار مقایسه هایی بین طلای دو بعدی و اولین ماده دو بعدی که تاکنون ایجاد شده است - گرافن ، که در سال 2004 در دانشگاه منچستر ساخته شد - وجود خواهد داشت.
وی گفت: "ترجمه هر ماده جدید به محصولات در حال کار می تواند مدت زیادی طول بکشد و شما نمی توانید آن را مجبور به انجام همه کارهایی کنید که دوست دارید. تست های محک استاندارد آشکار کرد که ورقه های نانو مقیاس طلا ده برابر بیشتر از نانوذرات طلا که معمولاً در صنعت استفاده می شوند ، کارآمد هستند.با گرافن ، مردم تصور کرده اند که این می تواند برای الکترونیک یا برای پوشش های شفاف خوب باشد - یا به عنوان نانولوله های کربنی که می توانند آسانسوری بسازند که به دلیل قدرت فوق العادهاش ما به فضا ببرد.
"من فکر می کنم با طلای دو بعدی ما ایده های کاملی درباره مکان استفاده از آن ، به ویژه در واکنش های کاتالیزوری و واکنش های آنزیمی ، به دست آورده ایم. ما می دانیم که این از فناوریهای موجود مؤثرتر خواهد بود - بنابراین ما چیزی را داریم که معتقدیم مردم علاقه مند به توسعه آن با ما خواهند بود."
ته نشست های طلای نوع کارلین در نوادا ایالات متحده آمریکا منشأ پنج درصد از تولید جهانی و 75 درصد از تولید طلای آمریکا است. در این ته نشست ها ، طلا به صورت تکه فلز ها یا رگه ها رخ نمی دهد ، بلکه - همراه با آرسنیک - در پیریت مخلوط شده است که همچنین به عنوان "طلای آدم نادان" نیز شناخته می شود. تیمی از دانشمندان از مرکز هلمهولتز پستدام - مرکز تحقیقات علوم زمینی آلمان GFZ - اکنون برای اولین بار به صورت آزمایشی نشان داده است که غلظت طلا به طور مستقیم به محتوای آرسنیک موجود در پیریت بستگی دارد. نتایج در ژورنال پیشرفت های علوم منتشر شده است.
منبع: دانشگاه لیدز و GFZ GeoForschungsZentrum Potsdam ، مرکز
تمام مواد از اتمها ساخته شدهاند. هر ماده (اکسیژن ، سرب ، نقره ، نئون و ...) دارای تعداد منحصر به فردی از پروتونها، نوترونها و الکترونهاست. به عنوان مثال اکسیژن دارای 8 پروتون، 8 نوترون و 8 الکترون است. هیدروژن دارای 1 پروتون و 1 الکترون است. اتمهای منفرد میتوانند با سایر اتمها ترکیب شوند تا مولکولهایی را تشکیل دهند. مولکولهای آب حاوی دو اتم هیدروژن H و یک اتم اکسیژن O هستند و از نظر شیمیایی H2O نامیده میشوند. اکسیژن و نیتروژن مهمترین اجزای هوا هستند و در طبیعت به عنوان مولکولهای دیاتومیک (دو اتمی) رخ میدهند. صرف نظر از نوع مولکول، ماده به صورت عادی به صورت جامد، مایع یا گاز وجود دارد. ما این خاصیت ماده را فاز یا حالت ماده مینامیم. سه حالت عادی ماده دارای خصوصیاتی منحصر به فرد هستند.
حالات ماده مرزهای بین مراحل مختلف ماده را مشخص میکنند و با سازمان و ترکیب فیزیکی ماده در ارتباط هستند. آنها اشکال مختلفی را که ماده در آنها وجود دارد تعریف میکنند. بگذارید نگاهی به حالات مختلف ماده بیندازیم و سعی کنیم فرآیندهای انتقال فاز را درک کنیم.
جامد:
هنگامی که در حالت جامد قرار داریم، مولکولهای یک ماده کاملاً به یکدیگر متصل هستند. از آن جا که مولکولها دارای موقعیت ثابت در فضا هستند، یک جامد، سفت و سختی را از خود نشان میدهد و شکل مشخصی دارد. فاصله بین مولکولی در حالی در یک جامد کمترین است که نیروهای بین مولکولی دارای قویترین جاذبه هستند. هنگامی که برای یک ماده در حالت جامد آن قدر گرما تأمین شود که دمای آن تا نقطه ذوب آن بالا برود، این ماده حالت مایع به دست میآورد. استثناء این قاعده در صورتی است که ماده جامد یک ماده عالی باشد. جامدی که در گرمایش مستقیماً حالت گازی را به دست میآورد به عنوان عالی شناخته میشود. کافور نمونهای از مواد عالی است. نمونههایی از مواد جامد شامل چوب، آهن، یخ، سنگ و غیره است.
مایع:
نیروهای جاذبه بین مولکولها در یک مایع کمتر از آنهایی است که در یک جامد وجود دارند و بیشتر از آنهایی است که در یک گاز وجود دارند. یک ماده در حالت مایع شکل مشخصی ندارد. شکل آن با شکل ظرف ماده مشخص میشود. هنگامی که یک مایع به نقطه جوش خود برسد، حالت گازی به دست میآورد. اگر با خنک کردن آن، گرما از یک مایع خارج شود، با رسیدن به نقطه انجمادش، به حالت جامد تغییر میکند. نمونههایی از مایعات شامل آب، خون، جیوه، شیر و غیره است.
گاز:
در این حالت، مولکولهای گاز در حالت حرکت تصادفی قرار دارند. آنها کمترین نیروهای بین مولکولی جاذبه را نشان میدهند و از این رو گازها شکل مشخصی ندارند. فواصل بین مولکولی بسیار زیاد است که به موجب آن ذرات گازها به طور گستردهای از یکدیگر جدا میشوند. چگالی و چسبندگی گاز نسبت به مواد جامد و مایعات کمتر است. مولکولهای گازی در برابر تغییرات دما و فشار بسیار آسیب پذیر هستند. هنگامی که یک گاز خنک میشود، حالت مایع به دست میآورد که سپس در خنک کنندههای بیشتر حالت جامد به دست میآورد. نمونههایی از گازها شامل هوا، بخار آب، هلیوم، ازن و غیره است.
به ما به طور کلی در مورد سه حالت ماده که در بالا ذکر شد آموزش داده میشود. این نسبتاً کمتر شناخته شده است که ماده در واقع در بیش از سه حالت مجزا وجود دارد. در این جا چهار مورد دیگر وجود دارد که ارائه میشود.
پلاسما:
گازی که از یونهای آزاد شناور تشکیل شده است به عنوان پلاسما شناخته میشود. یونهای شناور آزاد معمولاً اتمهایی هستند که به دلیل از دست دادن برخی از الکترونهای خود دارای بار مثبت خالص هستند. یونها همچنین میتوانند به شکل الکترونهای آزاد باشند. در شرایط ایجاد پلاسما، خود اتمها شروع به تجزیه میکنند، الکترونها از مدار خود دور هسته جدا میشوند و یونی با بار مثبت را پشت سر خود باقی میگذارند. مخلوط حاصل از اتمهای خنثی، الکترونهای آزاد و یونهای بارشی، پلاسما نامیده میشود. بنابراین، بارهای مثبت و منفی میتوانند به طور مستقل حرکت کنند و مولکولهای پلاسما را که به صورت الکتریکی رسانا هستند تشکیل دهند. پلاسما شکل مشخصی ندارد و به صورت ابرهایی شبیه گاز است. از آن جا که خواص پلاسما کاملاً متفاوت از مواد جامد، مایعات و گازها است، پلاسما به عنوان یک حالت جداگانه از ماده در نظر گرفته میشود. نمونههایی از پلاسما عبارتند از: شفق شمالی، قوسهای جوشکاری و صاعقه.
چگالیده بوز-انیشتین:
ماده در این حالت، مادهای است متشکل از بوزونهای خنک شده تا دماهای نزدیک به صفر مطلق. در این حالت، بیشتر اتمها به پایینترین حالت کوانتومی پتانسیل خارجی فرو میریزند. در این شرایط ، اثرات کوانتومی در مقیاس بزرگتر دیده میشوند.
سیال فوق بحرانی:
دما و شرایط تحت فشار که در آن مرزی بین فازهای ماده وجود ندارد، به عنوان نقطه بحرانی یک ماده شناخته میشود. هنگامی که یک ماده در دما و فشار بالاتر از نقطه بحرانی خود قرار دارد، به این عنوان شناخته میشود که در حالت فوق بحرانی قرار دارد. حالات ماده مرزهای بین مراحل مختلف ماده را مشخص میکنند و با سازمان و ترکیب فیزیکی ماده در ارتباط هستند.در این حالت، یک ماده خاصیت انتشار را با گازها به اشتراک میگذارد و خاصیت حل کنندگی مایعات را اتخاذ میکند.
ماده رو به انحطاط:
در این حالت، ماده دارای چگالی بسیار بالایی است. فشاری که ماده انحطاطی حفظ میکند تحت عنوان فشار انحطاط شناخته میشود. غالباً در این حالت، چگالی زیاد است. افزایش دمای ماده رو به انحطاط تأثیر کمی در فشار کل آن دارد. در دماهای بسیار بالا، فشار حرارتی افزایش مییابد. یکی از نمونههای شناخته شده ماده انحطاطی ماده عجیب است که گمان می رود در ستاره های نوترونی وجود داشته باشد.
آنچه در مورد حالات مختلف ماده جالب است تنوع گسترده در اشکالی است که یک ماده میتواند در آن حالات به خود بگیرد. به آن فکر کنید و خواهید فهمید که چگونه یک ماده مشابه در چهار یا پنج شکل مختلف میتواند وجود داشته باشد و خصوصیات فیزیکی مختلفی از خود نشان دهد. جالب است بدانید که چگونه شرایط دما و فشار باعث انتقال در حالات مختلف موادی میشود که جهان ما را تشکیل میدهند.
منبع: مانالی اوک

آبکاری روی یکی از محبوبترین روشهایی است که مورد استفاده قرار میگیرد. آبکاری فرایندی بسیار مقرون به صرفه بوده و عمدتا به منظور ارائهی پوششهای محافظ برای مواد فلزی مانند مهرهها، پیچها، اتصالات، قطعات اتومبیل و بسیاری دیگر از اقلام از آن استفاده میشود. علاوه براین مزایا، استفاده از روی باعث بهبود ظاهر کلی فلزات شده و با ارائهی انواعی از رنگها و حالتی روشن و درخشان ظاهری زیبا ایجاد خواهد شد.
در اینجا جزئیات بیشتری در رابطه با فرایند آبکاری و مراحل درگیر در فرایند آبکاری روی را ذکر میکنیم.
آبکاری فرایند پوششدهی یک فلز با فلز دیگر با استفاده از برق بوده که عمدتا به منظور ارائهی حفاظت از خوردگی انجام میگیرد. با استفاده از فرایند آبکاری قادر به تغییر صفات شیمیایی و فیزیکی یک فلز هستیم. آبکاری توسط فرایند گالوانیزه کردن انجام شده و شامل تشکیل سلول الکترولیت متشکل از کاتد و آند غوطه ور شده در محلول الکترولیت میباشد. در این مرحله فلز درون محلول آبی حاوی یونهای فلزی غوطه ور میشود. هنگامیکه جریان مستقیم به محلول آبی اعمال میشود، فلز در آند شروع به حل شدن میکند و یونهای فلزی آزاد به منظور تشکیل یک لایه نازک از پوشش بر روی شیء به کاتد وارد میشوند. شیء آبکاری شده، سوبسترا نیز نامیده میشود. فلز روی عمدتا به منظور ارائهی آبکاری برای فلزات فولاد و آهن مورد استفاده قرار میگیرد، هرچند که بسیاری از فلزات دیگر نیز با استفاده از روی آبکاری میشوند.
فرایند آبکاری روی شامل تشکیل یک لایه الکترولیت متشکل از دو فلز که الکترودها را تشکیل میدهند و عبور جریان الکتریکی به الکترولیتها میباشد. در حالیکه فلز روی، آند را تشکیل میدهد، فلزی مانند فولاد موضوعِ آبکاری کاتد را تشکیل میدهد. هنگامیکه جریان الکتریکی از محلول آبی عبور میکند، یونهای روی از طریق محلول آبی حرکت کرده و به سطح سوبسترا متصل شده و یک صفحه نازک را تشکیل میدهند. فرایند تشکیل صفحه فلز روی در انواعی از محلولهای آبی مانند محلولهای سیانید قلیایی، غیر سیانید قلیایی یا محلول نمک اسید کلرید انجام میشود.
مراحل آبکاری روی
اگرچه این فرایند ممکن است بسته به نیاز، سوبسترا، هزینه و نوع هدف درسطح تجاری متنوع باشد، اما معمولا مراحل اصلی آن به شرح زیر میباشد:
مرحله 1
تمیز کردن سوبسترا
تمیزکردن سوبسترا به منظور حذف هر گونه گرد و غبار، چربی و غیره از سطح انجام میشود. یک ماده شوینده قلیایی به منظور تمیز کردن سطح و تضمین کیفیت خوب آبکاری و سالم ماندن صفحه آبکاری شده برای دورهی طولانی مدت مورد استفاده قرار میگیرد. فرایند تمیز کردن نامناسب معمولا منجر به ارائهی آبکاری نامناسب، مانند لایه برداری از سطح آبکاری شده در طول زمان، میگردد.
فرایند تمیز کردن یک شیء شامل دو مرحله میباشد: حمام قلیایی و آبکاری. خیساندن فلز در حمام قلیایی برای مدت 5 تا 10 دقیقه در دمای حدود 150 درجه فارنهایت معمولاً برای رهایی از اکثر گرد و غبار و خاکهای موجود بر روی صفحه کافی میباشد. بعد از این مرحله، این بخشها با یک پاک کنندهی الکتریکی به میزان بیشتری تمیز میشوند. بار الکتریکی یا در انتهای کاتد و یا آند به فلز اعمال شده که منجر به انتشار اکسیژن یا هیدروژن از محلول و تمیز شدن قطعات سطح کوچک میگردد. فاکتورهای زمان و دما برای فرایند خیس خوردن قلیایی به یک اندازه مهم میباشد.
مرحله 2
فعال سازی یا قطعه شویی سوبسترا
فعال سازی فلز شامل حذف اکسیدها و فلسها از سطح با استفاده از محلولهای متنوع اسیدی میباشد. این لایههای اکسیدها و فلسها بر روی سطح فلز در طول فرایند تولید آنها و یا در هنگام ذخیره سازی و حمل و نقل تشکیل میگردد. قطعه شویی معمولا با استفاده از اسیدهایی مانند اسید سولفوریک یا هیدروکلریک اسید انجام می شود. نوع فلز و ضخامت فلسهای موجود بر روی فلزات میتواند نوع اسید، زمان غوطه ور شدن و دمای مورد نیاز برای فرایند فعال سازی را تعیین کند.
مرحله 3
آبکاری روی
تمیز کردن و فعال سازی مناسب قطعات تضمین میکند که آنها برای آبکاری با فلز روی آماده هستند. بخشهای فلزی ابتدا با آب شسته شده و سپس آنها را در یک محلول آبی مانند سیانید قلیایی قرار میدهند. سپس جریان مستقیم در آند برای یک زمان ثابت اعمال میگردد. این امر منجر به رسوب یونهای فلزی در کاتد یعنی سطح فلزی میگردد. مزیت اصلی آبکاری روی مقرون به صرفه بودن و سهولت کاربرد آن میباشد.برای دستیابی به آبکاری یکنواخت، ضروری است که آند و کاتد به صورت مناسبی در محلول آبی قرار بگیرند و جریان به صورت یکنواخت بر روی کل منطقه سطح فلزی عبور کند. در صورتیکه جریان یکنواخت نباشد، منجر به ضخیم شدن لایههای صفحات فلز روی بر روی مناطقی که مقدار بیشتری جریان را دریافت میکنند، میگردد، در حالیکه در مناطق دیگر لایههای نازکتری ایجاد میگردد.
انواعی از عوامل شیمیایی همراه با آبکاری روی به منظور دستیابی به خصوصیات فیزیکی و شیمیایی مورد نظر محصول نهایی مورد استفاده قرار میگیرد. این ویژگیها میتواند توسط تغییرات مناسب در عوامل شیمیایی مورد استفاده، دورهی زمانی غوطه ور سازی، بار الکتریکی اعمال شده و فاکتورهای زمان و دما تغییر کند.
مرحله 4
شستشو و خشک کردن محصول نهایی
قانون کلی، شستشوی قطعات با آب بعد از هر مرحله فرایند آبکاری میباشد. بعد از این که فلز آبکاری شد، به منظور حذف هر گونه آلایندههای موجود بر روی سطح آن در یک ظرف آب شستشو داده شده و سپس خشک میگردد. در مورد آلودگیهای بیشتر، شستشو با آب ممکن است چندین مرتبه انجام شود. قطعات بسته به سطح آلودگی و میزان آب مورد نیاز جهت جذف آلایندهها در یک مخزن شستشو و یا زیر جریان آب قرار داده میشود.
مزایا و معایب آبکاری روی
مزیت اصلی آبکاری روی مقرون به صرفه بودن و سهولت کاربرد آن میباشد. فرایند آبکاری روی، فلزی با ظاهری مناسب در انواعی از رنگها را ارائه میدهد. این فرایند میتواند به عنوان یک زیرلایه برای رنگها نیز مورد استفاده قرار گیرد. آبکاری از تشکیل زنگ سفید در طولانی مدت جلوگیری کرده و ویژگیهای شکلپذیری و چسپندگی عالی را ارائه میدهد.
محدودیتهای این فرایند آبکاری شامل کمبود دوام در آب دریا و عدم توانایی آن به منظور تشکیل ضخامت یکنواخت به دلیل شکل فلز آبکاری شده میباشد. این فرایند به آسانی پوششی را بر روی بخشهای خارجی فلز ایجاد میکند، اما به سادگی به نواحی داخلی شیء متصل نمیگردد.
منبع: Swapnil Srivastava - ScienceStruck

آلیاژ به عنوان ترکیبی از دو یا چند عنصر که حداقل یکی از آنها فلز است، تعریف میشود. آلیاژ میتواند ترکیبی از دو یا چند فلز یا ترکیبی از یک فلز یا چند فلز با نافلزات باشد. جزء یا فلز اصلی در یک آلیاژ، به عنوان فلز اصلی یا فلز پایه مورد اشاره قرار میگیرد. بر همین اساس، هدف از ایجاد آلیاژ این است که ترکیبی از این عناصر فلزی و نافلز، ویژگیهای خاصی را ارائه دهند. برای مثال، فولاد ضدزنگ که آلیاژی از فولاد و کروم است، برخلاف فولاد دچار زنگ زدگی یا خوردگی نمیشود. بخشهای زیر برخی از آلیاژهای رایج را ذکر میکند.
فهرست آلیاژها
برخی از فلزات شناخته شده مانند آلومینیوم، کبالت، مس و غیره دارای بیش از 5 نوع آلیاژ هستند. هر فلز دارای حداقل یک آلیاژ است. اکثر این آلیاژها برای اهداف صنعتی مورد استفاده قرار میگیرند. در این جا فهرست کوتاهی از آلیاژهای برخی فلزات را ذکر میکنیم.
آلومینیوم
AA-8000
آلنیکو (آلومینیوم، نیکل و مس)
دورالومین ( آلومینیوم، مس)
زاماک (روی، آلومینیوم، منیزیم، مس)
سیلومین (آلومینیوم، سیلیکون)
آلومینیوم آلیاژهای دیگری را با منیزیم، منگنز و پلاتین تشکیل میدهد.
بیسموت
فلزات چوبی (بیسموت، سرب، قلع، کادمیوم)
فلزات میدانی
فلز قرمز (بیسموت، سرب، قلع)
کبالت
ستیلیت (کبالت، کروم، تنگستن یا مولیبدن، کربن)
تالونیت (کبالت، کروم)
اولتیمت (کبالت، کروم، نیکل، مولیبدن، آهن، تنگستن)
ویتالیم
مگالیم
مس
آرسنیک مس
بریلیم مس (مس، بریلیم)
برنج (مس، روی)
بیلون (مس، نقره)
بروزن (مس، قلع، آلومینیوم یا هر عنصر دیگر)
کنستانتان (مس، نیکل)
کونیف (مس، نیکل، آهن)
مس – تنگستن (مس، تنگستن)
کوپرونیکل (مس، نیکل)
آلیاژهای سیمبال (مس، قلع)
الکتروم (مس، طلا، نقره)
آلیاژ هوسلر (مس، منیزیم، قلع)
هپازتیزون (مس، طلا، نقره)
منگانین (مس، منگنز، نیکل)
نقره نیکل (مس، نیکل)
شاکودو (مس، طلا)
طلای شمالی (مس، آلومینیوم، روی، قلع)
طلا
تومباگا (طلا، نقره)
الکتروم (طلا، نقره، مس)
طلای سفید (طلا، نیکل، پالادیم یا پلاتین)
طلای سرخ (طلا، مس)
آهن
آهن آنتراسیت (کربن)
آهن ریخته گری (کربن)
آهن قالب گیری (کربن)
آهن ورزیده (کربن)
آلیاژهای فرو
فولاد (کربن)
فولاد سیلیکون (سیلیکون)
فولاد ضد زنگ (کروم، نیکل)
فولاد ابزاری (تنگستن یا منیزیم)
کرومولی (کروم، مولیبدن)
سرب
سرب آنتیمونیال (سرب، آنتیموان)
لحیم (سرب، قلع)
مولیبدو چالکوس (سرب، مس)
نوع فلزی (سرب، قلع، آنتیموان)
نیکل
آلومل (نیکل، منگنز، آلومینیوم، سیلیکون)
کوپرونیکل (نیکل، برنز، مس)
کرومال (نیکل، کروم)
نقره آلمانی (نیکل، مس، روی)
هستلوی (نیکل، مولیبدن، کروم، برخی مواقع تنگستن)
فلز آلیاژ مونل (مس، نیکل، آهن، منگنز)
اینکونل (نیکل، کروم، آهن)
روی
زاماک (روی، آلومینیوم، منیزیم، مس)
آلیاژهای متعددی وجود دارد که معمولا در صنایع مختلف مورد استفاده قرار میگیرد. اساسا، در یک آلیاژ، خواص جزء یا فلز اصلی توسط ترکیب آن با اجزاء فلزی یا نافلزی دیگر افزایش مییابد.
در واقع آلیاژ یک واژه فرانسوی است که نام دیگر آن همجوشه می باشد. در حالت کلی به مخلوط یک محلول جامد فلزی که درون آن یک فلز اصلی که به آن فلز پایه می گویند به همراه یک یا چند عنصر فلزی و غیرفلزی است آلیاژ گفته می شود.

تنگستن
تنگستن فلزی خاکستری رنگ است و اکثراً به فرم ترکیب و در ترکیب با انواع دیگر از عناصر شیمیایی وجود دارد. تنگستن دارای چگالی بالایی بوده و 3/19 برابر چگالتر از آب و 71 درصد چگالتر از سرب میباشد. همچنین چگالی بیشتری نسبت به فلز اورانیوم دارد. از آنجا که عمدتاً دارای ناخالصیهای جزئی میباشد، تنگستن خالص در فرم عنصری آن شکلپذیری بهتری داشته و به طور گسترده در کاربردهای الکتریکی مورد استفاده قرار میگیرد. آلیاژهای تنگستن نیز در ساخت رشتههای لامپهای نوری تابان، لامپهای اشعه X و در ساخت آلیاژهای فوق العاده استفاه میشود.
اوسمیم
اوسمیم یک فلز واسطه متعلق به خانواده پلاتین است و به عنوان یکی از چگالترین عناصر موجود در طبیعت در نظر گرفته میشود. چگالی اسمیم دو برابر سرب است و نسبت به ایریدیم نیز تاحدی چگالتر میباشد. چگالی این فلز برابر 59/22 گرم بر سانتیمتر مکعب میباشد. اوسمیم به رنگ خاکستری مایل به آبی است، هر چند که برخی مواقع انواع خاکستری مایل به سیاه آن نیز موجود میباشد، فلزی بسیار سخت و شکننده است و دارای نقطه ذوب بسیار بالایی میباشد. این موضوع باعث شده که پردازش آن بسیار مشکل باشد. اوسمیم فلزی بسیار درخشان است و حتی در شب درخشندگی و زیبایی خاصی دارد.
تیتانیم
اگرچه تیتانیم دارای چگالی پایینتری نسبت به تنگستن و اوسمیم است، اما این فلز به جهت استحکام بالا، نسبت بالای استحکام به وزن، شکلپذیری بالا، مقاومت به خوردگی و نقطهی دوب بالای آن شناخته شده است. نقطه ذوب تیتانیم بیش از 1650 درجه سانتیگراد است. این فلز دارای توانایی نسبتاً پایینتری جهت هدایت گرما و برق بوده و دارای خواص پارامغناطیسی نیز میباشد. تیتانیم به رنگ نقرهای بوده و درجات تجاری آن دارای استحکام کششی حدود 63000 پوند بر اینچ مربع میباشند.
خواص فلزات
فلز شیئی است که دارای برخی خواص فیزیکی و شیمیایی ویژه است که آن را از عناصر دیگر متمایز کرده و به عنوان یک فلز معرفی میکند. یک فلز میتواند یک عنصر خالص، ترکیب و یا آلیاژ باشد و مشخصترین ویژگی آن توانایی هدایت الکتریکی با از دست دادن آسان الکترونها و تشکیل یونهای مثبت میباشد. هر عنصر شیمیایی که دارای همهی خواص زیر باشد، به عنوان فلز شناخته میشود. این خواص منحصر به فرد در زیر تحت عنوان خواص فیزیکی و شیمیایی طبقه بندی شدهاند.
خواص فیزیکی:
خواص فیزیکی منحصر به فرد فلزات به شرح زیر میباشد:
* چگالی بالا: عناصر، ترکیبات و آلیاژهای فلزی دارای چگالی بالایی هستند که این موضوع بدین معنی است که آنها بر روی سطح آب شناور نمیمانند.
* نقطه ذوب بالا: فلزات نیازمند دماهای بسیار بالا به منظور ماندن به حالت مایع میباشند. جیوه تنها فلزی است که حتی هنگامیکه در دمای اتاق نگه داری میشود نیز به فرم مایع میباشد. در واقع، نقطه ذوب جیوه حدود 40 درجه سانتیگراد است که بالاتر از دمای اتاق میباشد.
* درخشندگی: فلزات و اشیاء فلزی هنگامیکه شدتهای نور بالا با سطح آنها برخورد میکند، به شکل اشیاء نورانی مشاهده میشوند.
* هدایت الکتریکی بالا: فلزات هدایت کنندههای عالی الکترسیته بوده و همین دلیل استفادهی گسترده سیمهای مسی در لوازم الکتریکی و ماشین آلات میباشد.
* هدایت گرمایی بالا: فلزات هدایت کنندههای خوب گرما بوده و این موضوع میتواند در سرعت هدایت گرما توسط آنها در هنگام تماس با آتش یا هر شیء داغ دیگر مشاهده شود.
* شکلپذیری: به جز جیوه، همهی فلزات در مقابل اعمال نیرو به شکل ورقههایی در آمده و تحت تنش شکسته نمیشوند.
* خواص شیمیایی: مهمترین ویژگی شیمیایی فلزات، توانایی آنها به منظور تشکیل یونهای مثبت یا کاتیونها توسط از دست دادن الکترونها میباشد. ویژگی دیگر برخی فلزات مانند آهن، نقره، مس، روی و نیکل این است که آنها با اکسیژن اتمسفری واکنش داده و اکسیدهایی را بر روی سطح خود تشکیل میدهند. این لایه اکسید همان چیزی است که ما به عنوان زنگ بر روی آهن و لکههای تیره بر روی نقره مشاهده میکنیم. یک فلز میتواند یک عنصر خالص، ترکیب و یا آلیاژ باشدفلزات خاصی مانند طلا، پلاتین، پالادیم در هیچ حالتی با اکسیژن واکنش نمیدهند، در حالیکه در برخی دیگر از فلزات مانند آلومینیوم، منیزیم و تیتانیوم، تحت برخی شرایط اکسیداسیونهای بازی به صورت تشکیل یک لایهی محافظ بر روی سطوح آنها قرار گرفته و از خوردگی فلزات جلوگیری میکند. اکسیدهای فلزی ماهیت بازی دارند، در حالیکه اکسیدهای غیر فلزی ماهیت اسیدی دارند.
سه فلز ذکر شده در شروع این مقاله مهمترین فلزات در جهان میباشند. همان طور که از بررسی خواص این فلزات مشاهده کردید، یک فلز ممکن است استحکام بالا و چگالی پایینی داشته باشد، در حالیکه فلزی دیگر دارای چگالی بالایی باشد، به همین دلیل هیچ فلزی همهی مزایا را با هم در اختیار ندارد. اما بر اساس بررسیهای صورت گرفته، قویترین فلز در طبیعت فلز طلا میباشد که حتی قدرتمندترین و تاثیرگذارترین مردان تاریخ نیز به دنبال جذابیت و زرق و برق آن از این فلز استفاده میکردند.
لازم به ذکر است عقیده بر این است که تیتانیوم فلزی برتر در صنایع پیشرفته محسوب میشود که از آن به طرز فزاینده ای در تولید پروتزها و مفاصل مصنوعی استفاده میشود. این فلز بسیار مستحکم، مقاوم و غیرسمی است. اما حالا دانشمندان دانشگاه رایس در آمریکا با ترکیب طلا و تیتانیوم از آلیاژ فلزی منحصر به فردی رونمایی کردهاند که مهمترین ویژگی آن استحکام خیره کنندهاش است.
امیلیا موروسن که هدایت دانشمندان در این پروژه را بر عهده دارد می گوید: آنچه که ما تولید کرده ایم بین 3 تا 4 بار سختتر از فولاد است.
استفاده از ترکیب مشخصی از تیتانیوم و طلا در این آلیاژ اوج هنرنمایی به کار رفته در تولید آن به حساب میآید. آنها در این ترکیب به ازای هر 3 واحد تیتانیوم، یک واحد طلا به کار گرفتهاند.
منبع: Ishani Chatterjee Shukla - ScienceStruck

هنگامیکه دو یا چند فلز یا نافلز با هم ترکیب میشوند و طی واکنشهای همجوشی، رسوب الکترولیتی و غیره در نهایت مخلوط میگردند، محصولی نهایی به نام آلیاژ را تشکیل میدهند که در مقایسه با فلز پایه، قویتر و بادوامتر است. فلزات مختلفی که به منظور تهیه آلیاژها استفاده میشوند شامل مس، قلع، آلومینیوم، کروم، نیکل، نقره و غیره میباشند. علاوه بر این، عناصر مختلف غیر فلزی مورد استفاده به منظور ساخت آلیاژ شامل کربن، بور، سولفور، روی و غیره میباشد. بسته به ترکیب فلز یا نافلز مورد استفاده در آلیاژ، ما میتوانیم انواع مختلفی از آلیاژها را تولید کنیم.
آلیاژهای مختلفی وجود دارد که از ترکیب فلزات و نافلزات تشکیل شدهاند. انواع مختلفی از فلزات آلیاژی مانند آلیاژهای باینری وجود دارد که توسط ترکیبی از دو ماده، یا دو فلز و یا یک فلز و یک نافلز تشکیل شده و آلیاژهای سه گانهای نیز وجود دارد که از ترکیب سه عنصر تشکیل شدهاند. برای تشکیل آلیاژ، وجود حداقل یک فلز ضروری است. در این مقاله ما برخی از انواع رایج آلیاژها و مصارف آنها را بیان میکنیم.
آلیاژ فولاد ضدزنگ و مصارف آنها
ترکیب
نام فولاد ضد زنگ معمولاً اشاره به آلیاژهای فلزی متشکل از 5/10 درصد یا بیشتر کروم و 50 درصد آهن در آن دارد. کروم موجود در فولاد ضد زنگ باعث ارائهی خواص مقاومت بالا به خوردگی در این آلیاژ میگردد. آهن خالص ناپایدار بوده و با تشکیل زنگ به طور طبیعی پوسیده میشود. با افزودن کروم، آهن از ترکیب اکسیژن و آب به منظور تشکیل زنگ جلوگیری میکند. انواعی مختلفی از فولاد ضدزنگ بسته به مقدار کروم، آهن و فلزات دیگر موجود در آنها وجود دارد.
| نوع فولاد ضد زنگ | ترکیب |
| مارتنزیتی | آهن، 12 تا 14 درصد کروم، 1/0 تا 1 درصد کربن، 2/0 تا 1 درصد مولیبدن |
| فریتیک | آهن، 11 تا 18 درصد کروم، 08/0 تا 2/0 درصد کربن |
| آستنیتی | آهن، 17 تا 25 درصد کروم، 10 تا 20 درصد نیکل، 15/0 تا 2 درصد کربن |
| داپلکس | آهن، 19 تا 28 درصد کروم، کمتر از 5 درصد مولیبدن، 1 تا 6 درصد نیکل |
از آلیاژ به منظور ساخت ظروف آشپزخانه استفاده میشود، چون فولاد ضد زنگ یکی از بهداشتیترین سطوح به منظور ذخیره سازی و تهیهی غذا میباشد. این آلیاژ فولادی تأثیری بر طعم مواد غذایی نداشته و در طی آشپزی با غذاهای اسیدی واکنش نمیدهد. علاوه بر این، از آن جا که بر روی سطوح فولاد منافذی وجود ندارد، بنابراین میکروبها، گرد و غبار یا هر گونه آلودگی را بر روی خود جمع نمیکند، بنابراین تمیز کردن آن بسیار آسان است. فلزات مختلفی که به منظور تهیه آلیاژها استفاده میشوند شامل مس، قلع، آلومینیوم، کروم، نیکل، نقره و غیره میباشند.علاوه بر ظروف آشپزخانه، فولاد ضد زنگ برای تهیه ابزار جراحی، میلههای تقویت کننده، ماشینهای ظرفشویی، کشتیها، تانکرهای شیمیایی و غیره نیز استفاده میشود.
آلیاژ برنج و مصارف آن
ترکیب
آلیاژ برنج توسط ترکیب روی و مس تشکیل میشود و دارای رنگ قهوهای مایل به قرمز روشن و تیره مایل به زرد میباشد. رنگ این آلیاژ بر اساس مقدار فلز روی موجود در آن متنوع میباشد. آلیاژ برنج بسته به ترکیب آن میتواند به چندین نوع تقسیم گردد. در اینجا برخی از انواع آلیاژهای برنج را ذکر کردهایم.
| انواع آلیاژ برنج | ترکیب |
| تیوبهای برنجی | مس، 28 درصد روی و 1 درصد قلع |
| برنج قرمز | مس، 5 درصد قلع، 5 درصد سرب و 5 درصد سرب |
| برنج زرد | مس، 33 درصد روی |
| برنج سفید | مس، کمتر از 50 درصد روی |
| برنج آلومینیوم | 76 درصد مس، 22 درصد روی، 2 درصد آلومینیوم |
| برنج نیکل | 70 درصد مس، 5/24 درصد روی و 5/5 درصد نیکل |
| برنج عاری از سرب | مس، روی و کمتر از 25/0 درصد سرب |
| برنج منگنز | 70 درصد مس، 29 درصد روی و 13 درصد منگنز |
آلیاژ برنج یک رسانای خوب گرما، مقاوم به خوردگی آب شور و غیره میباشد، به همین دلیل برای ساخت اقلامی که در تماس با محیطهای سخت مانند لولهها قرار دارند، استفاده میشود. خواص صوتی عالی آلیاژ برنج آن را برای ساخت ابزار موسیقی بادی مناسب ساخته است. ابزارهایی مانند آلات موسیقی بادی، ترومبون، ساکسوفون، شیپورهای بزرگ، کرنا و غیره از آلیاژ برنج ساخته میشوند. علاوه بر این، از آن جا که آلیاژ برنج به راحتی کدر رنگ نمیگردد، از آن جهت برای ساخت ظروف آشپزی، کارد و چنگال و وسائل تزئینی کوچک استفاده میشود. خواص هدایت حرارتی این آلیاژ آن را جهت ساخت رادیاتورها و مبدلهایی مانند خنک کنندههای روغن، دستگاه تهویه هوا و هستههای بخاریها مناسب ساخته است.
آلیاژ نقره استرلینگ و مصارف آن
ترکیب
نقره در خالصترین شکل خود دارای قابلیتهایی مانند چکش خواری و شکلپذیری بوده و بسیار نرم میباشد. این نرمی باعث سهولت کار با آن میگردد، هر چند که این ویژگی دارای معایبی نیز هست. این امر باعث شده تا نقره به راحتی تغییر شکل داده و بنابراین برای ساخت اقلامِ کاربردی مناسب نیست. بنابراین، نقره خالص در ترکیب با 5/7 درصد فلز مس باعث ایجاد آلیاژ نقره استرلینگ میگردد. در آلیاژ نقره استرلینگ علاوه بر مس، فلزاتی مانند ژرمانیوم، پلاتین و روی نیز وجود دارد.
نقره استرلینگ برای ساخت جواهرات نقره استفاده میشود. یکی دیگر از کاربردهای محبوب آلیاژ نقره استرلینگ استفاده از آن در ساخت کارد و چنگال می باشد. چاقوها، قاشق، چنگال و سینیهای نقرهای نیز با استفاده از آلیاژ نقره استرلینگ ساخته میشود. از آنجا که این آلیاژ به طور طبیعی ضد عفونی میباشد و به گندزداها، گندزدایی حرارتی و مایعات بدن مقاوم میباشد، در ساخت ابزارهای پزشکی مورد استفاده قرار میگیرد. علاوه بر این، از این آلیاژ در ساخت ابزار موسیقی مانند فلوت و ساکسوفون، نیز استفاده میشود.
این موارد ذکر شده در بالا تنها سه نوع از آلیاژهای موجود و کاربردهای آنها میباشد. به دلیل این که فرم خالص فلزات عمدتاً بسیار ظریف و حساس هستند و جهت ساخت اقلام کاربردی مناسب نیستند، استفاده از آلیاژها بسیار مفید است. با این حال، با تشکیل آلیاژ، ما قادر به استفاده از همهی فلزات هستیم.
منبع: Priya Johnson - ScienceStruck

از میان همهی عناصر در جدول تناوبی، تنها فلزات واسطه کبالت، نیکل و آهن قادر به تولید میدان مغناطیسی میباشند. فلزات واسطه شامل 38 عنصر در جدول تناوبی هستند که در گروه 3 تا 12 قرار دارند. این فلزات شکلپذیر و چکش خوار بوده و معمولاً ظاهری درخشان دارند. آنها رساناهای خوبی برای گرما و برق میباشند. این عناصر به دلیل حالات اکسیداسیون متنوع آنها که احتمالاً به واسطه حضور الکترونهای ظرفیت در بیش از یک لایه میباشد، به خوبی شناخته شدهاند.
اسکاندیم، کادمیوم، تیتانیوم، هافنیم، وانادیم، تانتال، کروم، تنگستن، منگنز، رنیم، آهن، اسمیم، کبالت، ایریدیم، نیکل، پلاتین، مس، طلا، روی، جیوه، ایتریم، رادرفوردیم، زیرکونیوم، دوبنیم، نیوبیم، سیبورگیوم، مولیبدن، بوهریم، تکنتیوم، هاسیم، روتنیم، مایتنریم، رودیم، دارمستادیوم، پالادیم، انبیوم، ان انیوم و نقره همگی جزو فلزات واسطه میباشند. خواص منحصر به فرد این عناصر باعث کاربرد آنها در ساخت بسیاری از اقلام از جمله تولید میخهای آهنی تا ساخت فضاپیما شده است. ما در اینجا به برخی از کاربردهای فلزات واسطه اشاره کرده و اهمیت آنها را در یک جامعه متمدن مورد بررسی قرار میدهیم.
کاربرد فلزات واسطه
آهن
آهن فراوانترین فلز واسطه موجود است و چهارمین فلز فراوان در جدول تناوبی میباشد. آهن کاربردهای بسیار مفیدی به ویژه هنگامیکه با عناصر دیگر به منظور تهیه آلیاژهایی مانند فولاد ترکیب میگردد، دارد. چنین آلیاژهایی دارای مصارف بسیار زیادی مانند تولید مواد ساختمانی، ابزارها، وسایل نقلیه، مواد آرایشی، رنگها، کودها و غیره بوده و اهمیت بالقوهای در اقتصاد جهانی دارند. از آهن ریختهگری معمولاً به منظور پوشش دادن کورهها استفاده میشود. آهن به عنوان یک کاتالیزور هنگام تولید آمونیاک مصنوعی در فرایند هابر مورد استفاده قرار میگیرد. مهمتر این که، آهن عنصری بسیار مهم در بدن بسیاری از حیوانات است که به منظور ایجاد هموگلوبین مورد استفاده جهت حمل اکسیژن در خون مورد استفاده قرار میگیرد.
اسکاندیم
اسکاندیم 25 بخش در میلیون از پوسته زمین را تشکیل میدهد. این عنصر معمولاً از معادن نادری به نام تورت وئیتیت یا هنگام فراوری اورانیوم از سنگهای معدنی متنوع استخراج میگردد. این فلز در صنعت ساخت تلویزیون به دلیل خروجی نور خوب آن که مشابه با طیف خورشیدی میباشد، استفاده میگردد. برخی از ایزوتوپهای اسکاندیم به منظور آنالیز نمونههای نفت خام استفاده میشود. آلیاژهای آلومینیوم هنگامیکه مقادیر کمی از اسکاندیم به آنها اضافه میگردد، تاحدی تقویت میگردند.
وانادیم
وانادیم یکی دیگر از عناصر فراوانی است که در بیش از 60 ماده معدنی یافت میگردد. این فلز به عنوان یک محصول جانبی در طول فرایند تولید اورانیوم و نفت خام یافت میشود. وانادیم در ایجاد آلیاژهای فولاد که قویتر و مقاومتر به فرسایش و خوردگی هستند، اهمیت داشته و به منظور ایجاد ابزارهای با سرعت بالا نیز مورد استفاده قرار میگیرد. برخی مواقع از این فلز به منظور اتصال فولاد و تیتانیوم استفاده میشود. اسکاندیم در صنایع شیمیایی برای تولید اسید سولفوریک نیز کاربرد دارد.
منگنز
منگنز سومین عنصر واسطه فراوان موجود میباشد. اکثر منگنزِ موجود، در کف اقیانوسهای سراسر جهان یافت میگردد. اکثر منگنزی که استخراج میگردد، در تولید فولاد استفاده میشود. بقیهی منگنز نیز به منظور ایجاد اجزاء دستگاههای الکترونیکی، به دلیل ضریب مقاومت به دمای پایین آنها کاربرد دارد. منگنز جهت ایجاد پتاسیم پرمنگنات که در آزمایشگاههای شیمی سراسر جهان استفاده میشود، نیز کاربرد دارد. منگنز در ساخت باطریهای خشک، تولید آجر و شیشه، کودها و تولید آهنرباهایی که در تلویزیون به کار میرود، نیز استفاده میشود.
کبالت
این عنصر نسبتاً کمیاب است و در درجه اول در ساخت سرامیک و صنایع رنگ به منظور ایجاد رنگهای آبی استفاده میشود. برخی از ترکیبات کبالت در ایجاد آلدهیدهایی که در صنعت شیمیایی مفید میباشد، نیز استفاده میشود. کبالت به منظور ساخت آلیاژهاى سخت جهت ساختن موتورهاى پیستونى نیز کاربرد دارد. این عنصر جهت تولید آلیاژهای مقاوم به دمای بالا که در ساخت توربینهای گازی استفاده میشود، نیز کاربرد دارد. آلیاژهای منگنز مانند فولاد آلنیکو با کمک کبالت تولید میشود.
نیکل
بخش عظیمی از تولید نیکل جهان مربوط به دهانه عظیم شهاب سنگهای موجود در سودبری کاناداست که این امر نشان میدهد که مواد معدنی در این ناحیه، از فضا منشأ گرفتهاند. نیکل در درجه اول به منظور تولید آلیاژهای آهن و غیر آهن مانند فولاد آلنیکو و فولاد ضدزنگ مورد استفاده قرار میگیرد. نیکل در فرایند تولید روغنهای گیاهی و مارگارین نیز استفاده میشود. این فلز در آزمایشگاههای شیمی و صنایع سراسر جهان نیز کاربرد دارد.
مس
مس یک عنصر بسیار مهم از نظر سیستمهای الکتریکی است که در ساخت سیمهای مسی استفاده میشود. این عنصر در ساخت سکههای ارز در بسیاری از کشورها استفاده میشود، در ساخت میلههای سبک، سیستمهای حرارت دهی و خنک کنندگی و غیره نیز کاربرد دارد. علاوه بر این، مس بخش مهمی از آلیاژهایی مانند برنج، برنز و مونل میباشد. همچنین، به دلیل چکش خواری و غیر واکنشپذیر بودن با آب، از مس به منظور ساخت لولههای آب، بخاریها و ظروف آشپزی استفاده میشود.
روی
بیش از 6 میلیون تن فلز روی سالانه تولید میگردد، این فلز بیشتر به منظور پوشش دادن فلزات مختلف جهت حفاظت از خوردگی و زنگ زدگی مورد استفاده قرار میگیرد. فلز روی در تولید باطریها و در فرایند ریخته گری نیز کاربرد دارد، یک جزء مهم از آلیاژهای برنج میباشد. بدون این فلزات، بشر همچنان در عصر حجر میبود.اکسید روی در تولید منسوجات، رنگها و محصولات پلاستیکی نیز استفاده میشود. روی سولفید در تلویزیونها، ساعتها و لامپهای با نور فلورسنت نیز استفاده میشود. این عنصر در ساخت سم موش کاربرد دارد. بدن انسان از عنصر روی به منظور التیام زخمها و ذخیره سازی انسولین درون پانکراس استفاده میکند.
نقره
نقره رسانای خوب الکترسیته بوده و در هنگام قرار گیری در معرض هوا یا آب خورده نمیشود. این فلز برای ساخت جواهرات و اتصالات الکتریکی به ویژه هنگامیکه با مس ترکیب میشود، مناسب میباشد. نقره فلزی بسیار مهم در فرایند تولید عکس بوده و در باطریهای کادمیومی نیز یافت میشود.
طلا
هر کسی میداند که طلا فلزی بسیار باارزش و گران قیمت میباشد. همانند نقره، فلز طلا نیز در معرض آب و هوا دچار خوردگی نمیشود و رسانای خوبی از الکترسیته میباشد. طلا در ساخت تراشههای کامپیوتر، سیمها، اتصالات الکتریکی و جواهرات مورد استفاده قرار میگیرد. برخی از ایزوتوپهای رادیواکتیو طلا نیز به عنوان ایمپلنت در درمان برخی سرطانهای خاص استفاده میشود.
پلاتین
در ابتدا، اکثر معدنچیان هنگامیکه در جستجوی طلا بودند، به پلاتین میرسیدند. امروزه، پلاتین معمولاً فلزی گرانتر و مفیدتر از طلا میباشد. این فلز به واسطه خواص دوام، مقاومت در مقابل کدر شدن و رنگ زیبای آن در ساخت جواهرات مورد استفاده قرار میگیرد. از پلاتین در ساخت سلولهای سوخت و نیتریک اسید استفاده میشود و به عنوان یک کاتالیزور در اتومبیلها به منظور کاهش انتشار آلایندههای کربن مونوکسید و اکسیدهای نیتروژن کاربرد دارد. پلاتین برخی مواقع در تولید دماسنجها و موتورهای موشک به واسطه توانایی آنها به مقاومت به دماهای بالا استفاده میشود. پلاتین میتواند در داروخانهها و در پزشکی نیز جهت تولید داروهای ضدسرطان و تجهیزات جراحی یافت شود.
کادمیوم
اگرچه کادمیوم فلز میباشد، اما به اندازهای نرم است که میتوان به راحتی آن را با چاقو برش داد. کادمیوم فلزی سفید مایل به نقرهای است که در آبکاری فلزات به منظور حفاظت آنها از خوردگی و زنگ زدگی استفاده میشود. این فلز در باطریها نیز یافت میشود. کادمیوم یک جزء مهم در میلههای کنترل کارخانههای هستهای به واسطهی ماهیت سریع آن در جذب نوترونها در طول فرایند همجوشی هستهای به شمار میرود.
جیوه
تنها فلز واسطهای که در دمای اتاق به حالت مایع باقی میماند، جیوه میباشد. جیوه عنصری است که در ساخت دماسنجها و همچنین بسیاری از دستگاههای اندازه گیری مانند فشارسنجها، هیدرومترها و پیرومترها نیز کاربرد دارد. این فلز به منظور حذف طلا و نقره از آمالگام استفاده شده و یک بخش از بسیاری از تنظیم کنندههای الکتریکی میباشد. به دلیل کاهش مقاومت آن برای جریان الکترسیته در دماهای بسیار پایین، جیوه گزینه بسیار مناسبی برای تحقیقات ابررساناها میباشد.
تیتانیم، زیوکونیم و هافنیم
تیتانیم نهمین عنصر فراوان موجود بر روی زمین و دومین فلز واسطه میباشد. تیتانیم یکی از قویترین و سبکترین فلزاتی است که توسط بشر تابه حال شناخته شده است. به واسطه استحکام کششی بالای آن، از این فلز در ساخت هواپیماهای جنگنده، ماشینهای مسابقه، فضاپیماها و دیگر وسایل نقلیهای که به طور منظم با نیروهای با فشار قوی و تنش مکانیکی مواجه میشوند، استفاده میشود. تیتانیم به منظور ایجاد اندامها و مفاصل مصنوعی برای افرادی با نقص فیزیکی نیز استفاده میشود. تیتانیم در ساخت لولههایی که بخشی از ایستگاههای برق هستهای هستند، نیز کاربرد دارد. ترکیبات این فلز در تولید رنگ سفید در سراسر جهان استفاده میشود.
زیوکونیم و هافنیم همیشه با هم یافت میشوند. در حالیکه زیرکونیم برای ساخت آهنرباهای ابررسانا، نیروگاههای برق هستهای، پوششهای کوره و دیگ و لوسیونهای مختلف استفاده میشود، هافنیم در ساخت لامپهای رشتهای و انواع الکترودها کاربرد دارد.
کروم و تنگستن
حدود 96 درصد از کروم جهان از بخشهایی از شوروی سابق، آفریقای جنوبی و فیلیپین حاصل میگردد. این فلز معمولاً در فرایند آبکاری برای فرایندهای حفاظت و زینتی استفاده میگردد. علاوه بر این، به واسطه دوام پایین آن در دماهای پایین، از کروم در ساخت آلیاژهای غیر آهنی نیز استفاده میشود. از کروم برای تقویت فولاد و تولید شیشههای رنگی نیز استفاده میشود. تنگستن نیز به منظور تقویت فولاد و ایجاد مقاومت در برابر حرارت عمدتاً به دلیل این که دارای نقطه ذوب بالایی است، استفاده میشود. این مشخصه در ساخت لامپهای نوری، موشک و کوره نیز مهم میباشد.
ایریدیم و اسمیم
هر دو عنصر به عنوان محصولات جانبی هنگامی که پلاتین از سنگ معدن استخراج میشد، کشف شدند. ایریدیم عمدتاً به منظور ساخت کریستالهای لیزر با درجه حرارت بالا و شمشهای پلاتین – ایریدیم مورد استفاده به عنوان اندازه گیری استاندارد یک کیلوگرم، استفاده میشود.
از طرف دیگر، اسمیم فلز سختی است که به سایش و پاره شدن مقاوم میباشد. قبل از تنگستن، اسمیم به عنوان رشته در لامپهای نوری مورد استفاده قرار میگرفت. امروزه، از فلز اسمیم در ابزارهای الکتریکی، سوزنهای گرامافون و نوک قلمهای خودنویس استفاده میشود.
پالادیم و رودیم
تقریباً همزمان با کشف اسمیم، دو فلز گذرای دیگر نیز کشف شد. پالادیم در درجه اول در صنعت جواهر سازی به دلیل مقاومت بسیار خوب آن در مقابل کدر شدن استفاده میشود. پالادیم هنگامیکه با طلای زرد ترکیب میگردد، تشکیل طلای سفید میدهد. این عنصر در استخراج هیدروژن نیز استفاده میشود، چون بیش از 900 برابر حجم خود میتواند هیدروژن را جذب کند.
نیوبیم و تانتال
نیوبیم عنصری است که ظاهری مشابه با فولاد دارد. پس از جلا دادن، این عنصر بیشتر مشابه پلاتین خواهد بود. این فلز واسطه برای تولید دستگاههای الکترونیکی، آلیاژها و جواهرات مناسب میباشد.
تانتال کمیابترین فلز میباشد. این فلز مقاومت بالایی به خوردگی شیمیایی دارد. بنابراین، در ساخت خازنها و دستگاههای جراحی استفاده میشود.
برخی از این فلزات واسطه در تولید شیشههای رنگی و کاربردهای شیمیایی مانند خالص سازی نفت خام استفاده میشوند. تحقیقات نشان میدهد که این فلزات بخش مهمی از درمان بیماریهایی مانند سرطان و ایدز را به خود اختصاص دادهاند. به غیر از این، فلزات واسطه نقش مهمی در جهان زنده دارند. میتوان گفت که بدون این فلزات، بشر همچنان در عصر حجر میبود. در واقع، به دلیل وجود این عناصر در بدن ما، زندگی بدون این عناصر غیر ممکن است. به واسطه این اهمیت، تقاضا برای عناصر واسطه بر روی این کره خاکی هرگز متوقف نخواهد شد.
منبع: Anuj Mudaliar - ScienceStruck

اشعهی مرگ
نیکلا تسلا در سال 1930 ادعا میکرد که یک ”اشعه مرگ“ اختراع کرده و از آن با نام Teleforce یاد میکرد. این ابزار قادر به تولید اشعهی قدرتمند از انرژی بود که برای انهدام هواپیماهای جنگی دشمنان، نظامیان خارجی، یا هر چیز دیگری میشد از آن استفاده کرد. البته ”اشعهی مرگ“ هرگز به تولید نهایی نرسید چون تسلا معتقد بود که با به کارگیری آن انهدام و محو کردن کشورها از روی کرهی خاکی بیش از پیش آسان میشد.
تسلا این طور میگفت که یک دولت با استفاده از این ابزار قادر به انهدام هر چیزی در محدودهی 22 کیلومتری خود خواهد بود… [و] دیوار قدرت مستحکمی ایجاد خواهد کرد که هر کشوری، کوچک یا بزرگ را علیه همهی ارتشها، هواپیماها و دیگر نیروهای نظامی غیرقابل نفوذ خواهد کرد.“ وی گفته بود که تلاشهایی برای سرقت این اختراع انجام شده است. چندین ناشناس وارد اتاق کار او شده و برگههای تحقیقاتی وی را بررسی کردهاند اما سارقان یا جاسوسان مورد نظر دست خالی برگشتهاند.
نوسان ساز تسلا
در سال 1898تسلا ادعا کرد که موفق به ساخت نوسانساز کوچکی شده که بعد از اتصال به دفتر کار و راهاندازی، تقریبا تمام ساختمان و اطراف آن را به لرزه درآورده است. به عبارت دیگر، با استفاده از این ابزار امکان شبیهسازی زلزله میسر میشد. با توجه به خطرات احتمالی که ساخت چنین ابزاری میتوانست ایجاد کند، تسلا سریعا یک چکش گرفته و شروع به تخریب آن کرده و به کارمندانش هم سفارش میکند در صورتی که از وجود چنین چیزی از آنها سوال شد، ادعای بیاطلاعی کنند. بعضی از نظریهپردازان معتقدند دولت امریکا همچنان از تحقیقات تسلا در مکانهایی مثل تاسیسات هارپ (HAARP) استفاده میکند.
سیستم برق رایگان
تسلا با دریافت کمک مالی از سوی شرکت JP Morgan در سال 1902-1901 اقدام به طراحی و ساخت ابزاری به نام برج Wardenclyffe در نیویورک کرد، یک ایستگاه انتقال بیسیم غولپیکر. مورگان فکر میکرد برج Wardenclyffe امکان ارتباطات بیسیم را در سراسر جهان فراهم خواهد کرد اما تسلا برنامههای دیگری برای آن در سر داشت.
تسلا با استفاده از نظریات خود مبنی بر استفاده از زمین برای ارسال سیگنالها، قصد داشت با استفاده از این برج اقدام به ارسال پیام، تماسهای صوتی و حتی ارسال عکسهای رادیویی از دریای آتلانتیک به انگلستان و به کشتیهای دریایی کند. اگر این پروژه موفق میشد، هر کسی میتوانست با فرو کردن یک میله در زمین، به الکتریسیته دسترسی داشته باشد.
متاسفانه، رایگان شدن برق سود سرشار شرکتهای تامین نیرو را از بین میبرد. و ضمنا وجود چنین سیستمی میتوانست وضعیت قدرتهای جهانی را به خطر بیاندازد چرا که به طور کلی صنعت انرژی را متحول میکرد. تصور کنید اگر جامعه نیازی به سوختهای فسیلی نداشت، دنیا چه شکلی پیدا میکرد؟ آیا قدرتهای بزرگ جهانی همچنان امکان کنترل کشورها را داشتند؟ مورگان از تامین مالی تغییرات مورد نظر تسلا امتناع کرد. این پروژه در سال 1906 به حال خود رها و هرگز عملیاتی نشد.
بشقاب پرنده
در سال 1911 نیکلا تسلا به روزنامه New York Herald گفت که در حال کار روی یک ”ماشین پرنده“ ضد جاذبه است. اظهارات تسلا:
”ماشین پرندهی من نه بال دارد و نه ملخ. شاید با دیدن آن روی سطح زمین هرگز تصور نکنید که این یک دستگاه پرنده است. با این وجود این ماشین با امنیت کامل قادر به حرکت در تمام مسیرهای هوایی است و با بالاترین سرعت ممکن است؛ شرایط بد آبوهوایی اثر منفی روی آن نداشته و چالههای هوایی یا جریانهای هوایی مکنده هم مشکلی برای آن ایجاد نخواهند کرد. این دستگاه در صورت تشخیص وجود چنین جریانهای هوایی نامناسبی قادر به ارتفاعگیری بوده و بالاتر از سطح آنها پرواز خواهد کرد. این دستگاه حتی در صورت وزش باد شدید قادر است برای مدتی طولانی به صورت ثابت در آسمان بماند. مکانیزم قدرت پرواز دستگاه من از قوانین حاکم بر پرواز پرندگان پیروی نکرده، بلکه یک حرکت مکانیکی ساده است.“
بشقاب پرندهی تسلا با سیستم رایگان انرژی کار میکرد، آن هم در زمانی که صنعت هوافضا و صنعت خودرو وابسته به نفت بود. این اختراع هم دچار سرنوشتی مشابه سیستم انرژی رایگان شد.
بالونهای هوایی پیشرفته
تسلا طرح پیشنهادی جالبی در زمینهی جابجایی مسافران داشت: بالونهای هوایی برقی، با فاصله 12 کیلومتری از سطح زمین، تنها در طی 3 ساعت قادر به انتقال مسافران از نیویورک به لندن خواهند بود. وی حتی فکر میکرد امکان تامین انرژی بالونهای از اتمسفر وجود دارد، و به همین خاطر بالونها برای تامین انرژی هرگز نیازمند توقف نخواهند بود.
بالونهای هوایی بدون سرنشین میتوانستند مسافران را به مقصدهای از پیش تعیین شده منتقل کرده یا از آنها برای حملات جنگی از راه دور استفاده کرد. متاسفانه هیچ کسی اعتباری برای این پروژه قائل نشد. هر چند امروزه شاهد پرواز پهپادهای بدون سرنشینی هستیم که عملیاتهای بمباران هوایی را انجام داده، هواپیمایی با سرعت مافوق صوت ساخته شده که سرعت فوقالعاده بالایی داشته و فضاپیماهای که میتوانند بالاتر از جو زمین به دور آن بچرخند.
بسیاری از مردم همواره از FBI به عنوان مظنون اصلی سرقت تمام کارها، پروژههای تحقیقاتی و اختراعات تسلا یاد میکردند. درستی این شایعه با درخواستهای اخیر قانون آزادی اطلاعات که FBI را تحت فشار قرار داده بود، ثابت شد.
.jpg)
«الکساندر گراهام بل» در 141 سال پیش و زمانی که فقط 29 سال سن داشت، نخستین تماس تلفنی موفق دنیا را برقرار کرد تا این افتخار برای همیشه به نام او ثبت شود.
در دهم مارس سال 1876 میلادی، نخستین مکالمه تلفنی میان «الکساندر گراهام بل» و دستیارش «توماس واتسن» با موفقیت انجام شد.
الکساندر اهل اسکاتلند بود، اما پس از اینکه دو برادرش در جوانی به سل مبتلا شدند و درگذشتند، زادگاه خود را به مقصد کانادا ترک کرد. وی پس از گذراندن دوران نقاهت، راهی ایالات متحده آمریکا شد.
بل تحصیلات آکادمیک چندانی نداشت، اما از آنجایی که پدر و پدربزرگش گفتاردرمان بودند، او هم از کودکی با این حرفه آشنا بود، به ویژه آنکه مادرش نیز از نعمت شنیدن بیبهره بود.
آشنایی بل با این حرفه سبب شد در آموزشگاه ناشنوایان شهر بوستون مشغول به کار شود و در کنار آن نیز به تئوریهای خود درباره ارتعاشات و ... بپردازد.
آشنایی او با توماس واتسن سبب شکلگیری فکر اختراع تلفن در ذهنش شد. بل درخواست خود برای «حق امتیاز» (پتنت) این اختراع را در 14 فوریه سال 1876 میلادی تسلیم اداره پتنتهای آمریکا کرد. این در حالی بود که تنها چند ساعت قبل مخترع دیگری به نام «الیشا گری» درخواست مشابهی به آن اداره ارائه کرده بود. بل کمتر از یک ماه بعد اولین پتنت برای تلفن را دریافت کرد و سه روز بعد اختراع خود را در معرض دید سرمایهگذاران، خبرنگاران و اهل فن با موفقیت آزمایش کرد.
طولی نکشید که صدها چالش حقوقی تازه، در رابطه با همین پتنت پیش روی بل قرار گرفت که از این تعداد پنج مورد به دادگاه عالی آمریکا کشیده شد. اما در نهایت صحت ادعاهای بل تایید شد و یکی از طولانیترین دعواهای حقوقی تاریخ آمریکا بر سر پتنت خاتمه یافت.
وی بعد از آنکه به خاطر اختراع تلفن به شهرت رسید، توانست در سال 1882 میلادی شهروند آمریکا شود.
شهرت او بعدها به حدی رسید که واحد استاندارد برای اندازهگیری شدت امواج صوتی در دهه 1920 میلادی «بل» نام گرفت. «دسیبل» هم که یکدهم بل محسوب میشود، رایجترین مقیاس برای اندازهگیری بزرگی صدا به شمار میرود.
همچنین وقتی بل در دوم اوت سال 1922 میلادی درگذشت، دو روز بعد، تمامی سرویسهای تلفتی در آمریکا و کانادا برای یک دقیقه کامل و همزمان با خاکسپاریاش به حالت تعلیق درآمدند. علاوه بر این، تیمی متشکل از 60 هزار اپراتور تلفن به احترام وی یک دقیقه سکوت کردند و هیچ تماس تلفنی را هم وصل نکردند تا 13 میلیون تلفن در قاره آمریکا برای یک دقیقه زنگ نخورند.
دیگر اختراعات بل: تلفن بیسیم، فلزیاب و قایق سرعتی
1ـ در سال 1880 بل نوعی تلفن بیسیم را اختراع کرد که با بهرهگیری از پرتوهای نوری، حرفها و صداها را انتقال میداد. او این اختراع خود را که فوتوفون (برگرفته از کلمات یونانی به معنای «نور» و «صدا») نامگذاری و اعلام کرد: «فوتوفون بزرگترین اختراعی است که تا الان انجام دادهام و حتی از تلفن نیز اهمیتش بیشتر است.» اختراع او در زمان خود پیشرفت بزرگی محسوب میشد اما چندین دهه بعد، تکنولوژی فایبر اوپتیک از راه رسید و اختراع بل را به کناری نهاد.
2ـ در سال 1881 و پس از سوءقصد به جیمز آبرام گارفیلد (بیستمین رئیسجمهور آمریکا)، شرایط جسمانی او رو به وخامت گذاشت، چون پزشکان مجبور بودند با دستها و ابزارهای غیراسترلیزه اقدام به کنکاش درون بدن وی کنند تا گلولهها را بیابند. بل که معتقد بود علم میتواند روشهای بهتری برای پیدا کردن موقعیت گلوله در بدن ارائه کند، نوعی ماشین الکترومغناطیسی را ابداع کرد که پیشتر روی برخی از مجروحان جنگی امتحان کرده بود.
به همین دلیل، دو بار به کاخ سفید فراخوانده شد تا از دستگاهش برای پیدا کردن گلولهها در بدن رئیسجمهور استفاده کند اما تلاش موفقی نداشت. چرا که سیمهای موجود درون تشک اختلالاتی ایجاد میکرد، از سوی دیگر پزشک مخصوص رییسجمهور فقط اجازه معاینه سمت راست بدن را به بل داد چون تصور میکرد گلوله در آن سمت است، در حالی که کالبدشکافی پس از مرگ گارفیلد نشان داد گلوله در سمت چپ بدن او بوده است.
3ـ بل در دهه 1890 میلادی فعالیتهایی را در حوزه هوانوردی آغاز کرد و حتی توانست تعدادی کایت چهارضعلی سرنشیندار طراحی کند. رؤیای او ساخت هواپیمایی بود که بتواند از سطح آب تیکآف کند و به پرواز درآید. این رؤیا به ساخت قایقهای پرسرعتی انجامید که میتوانست روی سطح آب جهش کند. یکی از این قایقها HD-4 نام داشت و توانست در سال 1919 میلادی رکوردشکنی کند و سرعت 112 کیلومتر بر ساعت را به ثبت برساند.

به ندرت می توان کسی را پیدا کرد که آلبرت انیشتین را نشناسد یا دستکم اسم او را نشنیده باشد. انیشتین یکی از مشهورترین و باهوش ترین انسان هایی است که این کره خاکی به خود دیده و کسی هنوز نتوانسته در زمینه ی علم به پای او برسد. انیشتین در حوزه ی ریاضی و فیزیک سرآمد دوران خود بود و با نظریه ی نسبیت و تئوری کوانتوم خود انقلابی در علم به پا کرد. اما علاوه بر این موضوعات چیزهای دیگری نیز در مورد این نابغه ی بی نظیر وجود دارد که کمتر کسی از آن ها باخبر است.
1- اگر چه در آن زمان هنوز شناسایی نشده بود اما بسیاری بر این باورند که آلبرت انیشتین به اختلال «طیف اوتیسم» مبتلا بود. برخی از رفتارهای عجیب و غیرطبیعی او در دوران زندگی اش مانند بیزاری از لمس شدن، مشکل داشتن در مراودات اجتماعی و سختی هایی که در دوران مدرسه داشت همه از نشانه هایی است که امروزه در زمره ی اختلالات اوتیسمی طبقه بندی می شوند.
2- این که انیشتین در فیزیک و ریاضی نابغه بود بدین معنا نیست که او در همه چیز عالی بوده باشد. انیشتین ویولون می نواخت اما همیشه با شمارش ریتم ها و نت ها مشکل داشت.
3- انیشتین بارها قبل از مرگ گفته بود که جسد او را بسوزانند اما بعد از مرگ، پاتولوژیستی به نام توماس هاروی مغز او را دزدید. هاوری بر این باور بود که مغز انیشتین کلید نبوغ وی بوده اما علی رغم مطالعات فراوان نتوانست چیزی در این مورد پیدا کند تا این که خانواده ی انیشتین از دزدیده شدن مغزش توسط هاروی باخبر شدند.
4- البته نکات جالب و خاصی در مورد مغز انیشتین وجود داشت که می توانست دلیل باهوش بودن وی در این حد بوده باشد. بخش هایی از مغز او نسبت به انسان های دیگر ضخیم تر بود که می توانست به این معنا باشد که ارتباط قوی تری میان نیمکره های مغز او وجود داشته است.
5- در سال 1947، او یک دست نوشته ی بسیار سری را همراه با رابرت اوپنهایمر، پدر بمب اتمی، در مورد این که در صورت تماس با موجودات فضایی چه باید کرد نوشت. برخی بر این باورند که انیشتین با نوشتن این دست نوشته می خواست به نحوی به مردم بگوید که او چیزهایی در مورد موجودات فضایی می داند که دیگران از آن ها بی خبرند. برخی هم این شایعه را پخش کردند که انیشتین به دلیل تماس با موجودات فضایی تا این حد باهوش شده است.
6- انیشتین اولین کسی نبود که قواعد نظریه ی نسبیت را کشف کرد اما اولین کسی بود که از آن به عنوان یک قانون فیزیکی استفاده نمود. 10 سال قبل از این که انیشتین تئوری نسبیت خود را به جهانیان عرضه کند، یک فیزیکدان آلمانی به نام هندریک لورنتز این ایده ها را در بوته ی آزمایش قرار داد اما فکر نمی کرد که این قوانین در زندگی واقعی نیز کاربرد داشته باشند.
7- اولین باری که انیشتین تئوری نسبیت خود را منتشر کرد کسی بحث های علمی او را جدی نگرفت.
8- ظاهراً وقتی که عکس معروف او در حالی که زبانش را بیرون آورده بود گرفته شد وی به شدت درمانده شده بود. این عکس در روز تولد 72 سالگی او گرفته شد و پس از یک شب طوانی که برای عکاسان لبخند دروغی زده بود تصمیم گرفت که این بار زبانش را برای عکاس درآورد.
9- شاید انیشتین بسیار جلوتر از زمان خود به دنیا آمده بود زیرا قبل از سن 30 سالگی، اکثر تالیفات و تئوری های مهمش را به انجام رسانده بود.
10- بدون شک انیشتین نبوغ ذاتی و ذهنی خاصی داشت ولی بر این باور بود که دلیل موفقیت و شهرتش این نبوغ نبوده است. به جای آن وی بر این باور بود که ثبات قدم و تلاش هایش باعث شد که وی از اطرافیانش با فاصله ای زیاد پیشی بگیرد.




